主な違い:拡散とは、分子がバルクモーションを必要とせずに、ある場所から別の場所に移動して移動するプロセスです。 流出は、分子がピンホールを通って高濃度の場所から低濃度の場所へと移動するプロセスです。
拡散と滲出という用語は、化学、物理学、生物学などの多くの科学で一般的に使用されています。 化学ではこれら二つの用語は気体の二つの性質です。 これら2つは、単にガスの基本とその特性を学んでいるだけの多くの人々を混乱させています。 拡散と流出は2つの異なる用語を意味する2つの異なる用語であり、互換的に使用されるべきではありません。 拡散とは、ガスが互いに混ざり合う能力のことをいい、一方、拡散とは、ガスが小さなピンホールを通過する能力のことをいいます。 拡散はまた、社会学、経済学および財政学において、人々、アイデアおよび価値観の拡散を指すために使用されています。
拡散とは、バルク運動を必要とせずに分子がある場所から別の場所に移動して移動するプロセスです。 拡散は、運動エネルギーのみを使用することによって分子を移動または混合させる。 「拡散」という言葉はラテン語の「diffundere」から派生することを意味します。 拡散において、分子は一定の運動状態にあり、そして運動エネルギーまたは熱エネルギーによって推進されるとき、それらは他の分子と混合する傾向があり、結果として不可分の混合物を生じる。 実用的なアプローチを取りましょう。1つのコンテナは、ソリッドパーティションを使ってAとBのセクションに分割されます。 最初のセクションは水で満たされ、2番目のセクションは赤い染料で満たされています。 今度は仕切りが持ち上がるとき染料および水は全容器を満たすことを試みる。 それから染料はゆっくりと水を赤く染めます、これは拡散です。
拡散は分子を高濃度領域から低濃度領域へシフトさせ、その結果全ての分子が混ざり合う。 すべての分子が均等に広がると拡散は止まります。 拡散は水に限定されず、分子がより多くのエネルギーと他の分子と混合する能力を有する気体状態において最もよく機能する。 拡散には、現象論的と原子論的の2つのアプローチがあります。 現象論的アプローチによれば、分子は高濃度の領域から低濃度の領域へと移動する。 原子論的アプローチでは、拡散は拡散粒子のランダムウォークによって起こると考えられており、拡散は熱エネルギーによって推進されてそれらを混ぜ合わせる。 拡散は、身体が必要とするミネラル、栄養素、エネルギーを生み出すのに重要な役割を果たします。

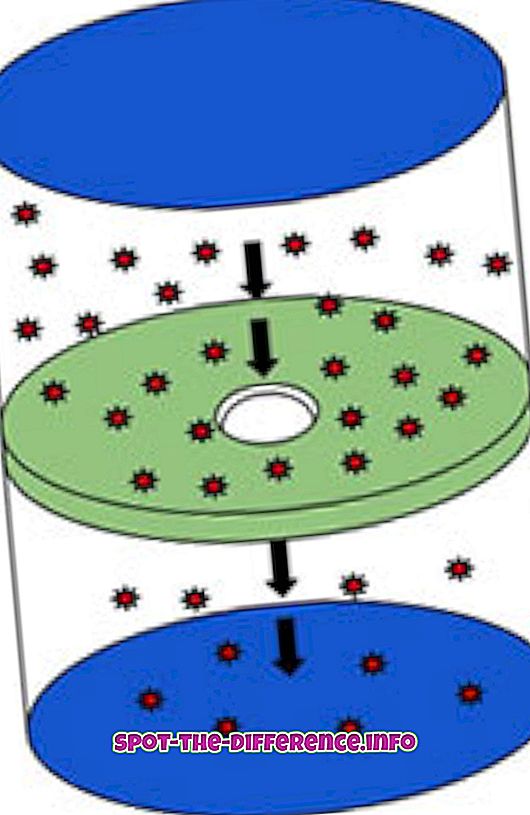
流出は、分子がピンホールを通って高濃度の場所から低濃度の場所へと移動するプロセスです。 このプロセスは、分子間の衝突なしにガスが小さな穴を通過する能力を表しています。 これは、穴の直径が分子の平均自由行程よりかなり小さいときに起こります。 平均自由行程は、連続する衝突の間に移動する粒子が移動した平均距離です。 これの実用的な例は容器を煙で満たして、瓶の小さな穴を突くことです。穴から穴をあけ始める煙は滲出液と考えられます。
スコットランドの化学者トーマス・グラハムは、滲出液を測定するための公式を作成したことによると、ガスの移動速度と測定方法を決定するグラハム則を作成しました。 グラハムの法則によると、ガスが流出する速度はそれらの分子量に依存する。 より低い分子量を有するガスは、より高い分子量を有するガスよりも早く流出する。 1秒間に何個の分子が穴を通過するかを測定することによって、流出量が計算されます。 同様に、熱力学では、ガスの噴出速度はその粒子の質量の平方根に反比例する。