主な違い:原子質量は、特定の同位体の質量、または原子の陽子、中性子、電子の合計質量です。 原子番号は、元素の核内にある陽子の数です。
化学は混乱している、元素の数、原子番号、結合、質量、重さ、原子など、混乱していることに直面しましょう。 原子質量と原子番号は、よく混同され互換的に使用される2つの単語です。
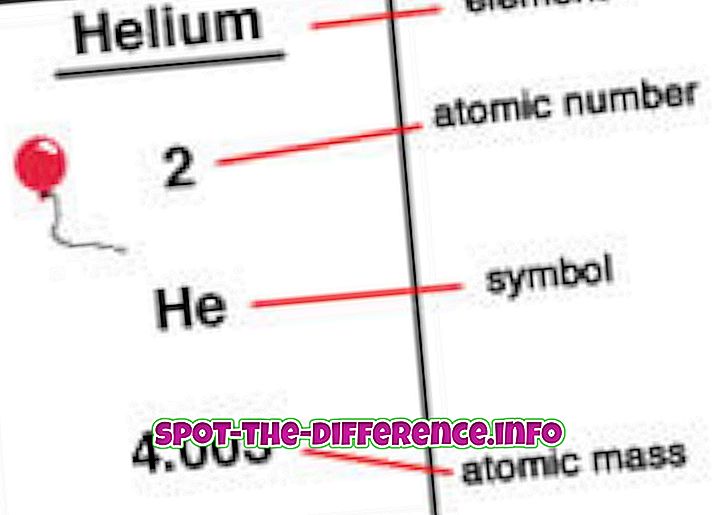
原子質量は、静止しているときの原子の質量です。 これは、原子が非常に速い速度で動いていると、質量が大きくなる傾向があるためです。 定義によれば、原子質量はすべての陽子、中性子、電子の質量ですが、電子は原子質量に大きな違いを作るには小さすぎます。 周期律表の元素のほとんどは同位体を持っており、中性子数の違いにより各同位体の質量も変化します。
原子量は原子量単位またはamuを使って表されます。 1原子質量単位は、炭素-12の質量の1/12に等しい。 原子の質量をCarbon-12の質量の12分の1で割ると、元素の相対質量が得られます。 ただし、オブジェクトの相対質量は、すべての同位体を考慮して計算されるため、実際には元素の原子量です。 とはいえ、これは元素の原子量とみなすべきではありません。

原子番号は、元素の核内にある陽子の数です。 原子が中性のとき、それは陽子と電子の数が同じであることを意味します。 原子番号はZで示されます。各元素は異なる数のプロトンを持っているので、この数は元素を表すのにも使われます。 同位体は通常同じ原子番号を共有しますが、それらの原子量を使用して分類されます。例えば、Carbon-12、Carbon-13です。
元素は周期表の原子番号順に並んでいます。 原子番号は、要素の左上隅に上付き文字として表示されています。 原子番号は元素についての情報を明らかにするのを助けることができます、そして多くの人々は原子番号を見て、それがどんな元素であるかを述べることができます。 また、周期表のどこに配置できるのか、また液体、気体、固体のいずれであるかを示します。 原子番号は、核の電荷、酸化状態、結合挙動、イオンの電荷などに関する情報も提供します。