主な違い :氷とドライアイスの両方がそれらの冷却特性に使用されます。 氷とドライアイスの主な違いは、それらの化学構造、性質、そして矛盾する温度にあります。
人々はよく似た外観と機能性のために、用語「氷」と「ドライアイス」と混同されがちです。 しかし、一方は水と接触すると蒸気を発散し、他方は単に水に溶けるので、氷とドライアイスは互いに大きく異なります。

それはさまざまな目的のために機械的に生成することができますが、氷は地球上に豊富にあります。 氷は、氷を作るために水を0℃以下に冷却することができる冷凍によって製造および貯蔵することができる。 市販の氷は、冬のレクリエーションやアイススケート、アイスホッケー、アイスフィッシングなどの多くのスポーツで広く使用されています。また、氷は気候や水循環において重要な役割を果たしています。

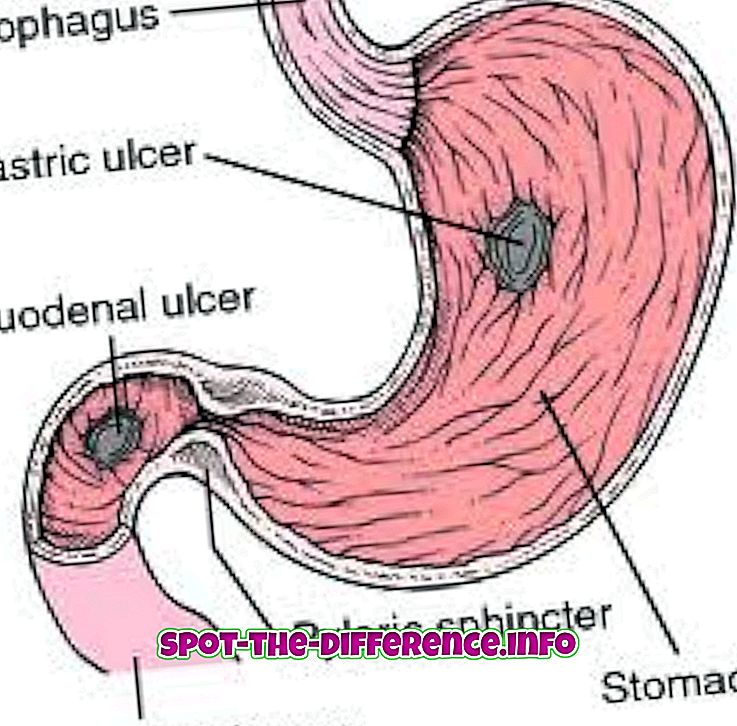
ドライアイスはカードアイスとも呼ばれ、主に冷却剤として使用されます。 それは本質的に無色であり、そして酸味の熱いにおいがする。 また、電気伝導性および熱伝導性が低く、不燃性および酸性を示します。 ドライアイスの超冷却特性と昇華技術は、それを非常に価値のある冷却剤にします。 ただし、ドライアイスは非常に慎重に取り扱ってください。毒性が強く、凍傷が発生する可能性があります。
ドライアイスは、何時間にもわたって高度の効率的な冷却を維持するので、アイスよりはるかに大きい冷却能力を提供する。 時々、それは通常の氷を使うことが必須ですが、与えられた製品の寿命を延ばすためにドライアイスも仕事に十分であることができます。 もう1つの重要な要素は、通常の氷は水に溶けやすいのに対し、ドライアイスは長持ちし、使用後もまったく残らないことです。
アイスとドライアイスの比較:
氷 | ドライアイス | |
化学構造 | H 2 Oは化学構造です。 | CO 2は化学構造です。 |
の形 | それは固体の形の水です。 | それは二酸化炭素の固体形です。 |
化学結合 | それは、2個の水素原子に共有結合した単一の酸素原子、またはHOHからなる。 | それは単一の炭素原子に結合した2個の酸素原子からなる。 |
州 | これには3つの状態があります。 固体 液体と ガス状 | それは直接固体から気体状態になります。 このプロセスは昇華と呼ばれます。 |
溶融 | それは熱を使って簡単に溶けることができます。 | それは大気圧を下げることによって溶かすことができます。 |
特徴 |
|
|
用途 |
|
|