主な違い :陽イオンと陰イオンは、原子または分子の一部です。 2つのイオン間の重要な違いは、それらのイオンの正味電荷であり、正イオンは正味負電荷を有し、負イオンは正味正電荷を有する。
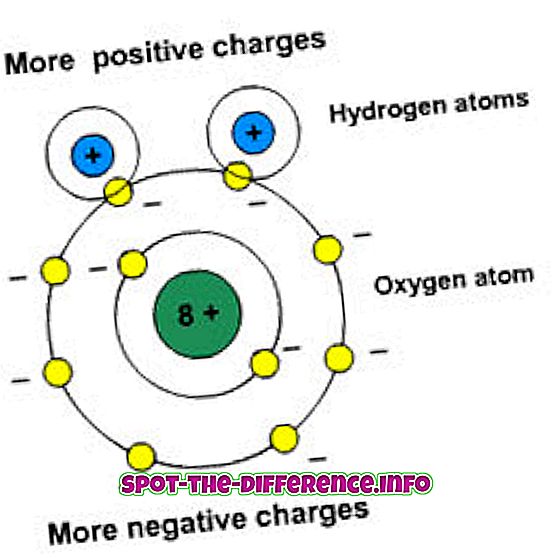
化学では、原子は物質の最小粒子であると考えられています。 そして、問題は宇宙全体が作り上げたものです。 それで、すべての物質、生きているまたは生きていない生物は原子で構成されています。 原子は、陽子、中性子、および電子で構成されている小さな原子核で構成されています。 陽子と中性子だけが原子の中に存在しているのに対して、電子は核の周りを専用の円軌道で回転しています。

イオンは分子または原子として定義され、ここで電子の総数はプロトンの総数と等しくなく、したがって原子に正味の正電荷または負電荷を与える。 ここで、イオンが電子の損失によって形成されると、正電荷が発生し、それが電子の獲得によって形成されると、負電荷が粒子に付与される。 このプロセス全体をイオン化と呼びます。
イオン化において、その上に正味の正電荷を有するイオンは、「陽イオン」または「陽イオン」と呼ばれる。 陽イオンは電子よりも陽子の数が多いイオンです。 中性イオンが価電子殻から一個の電子を失い、核内の陽子数が外殻内の電子数よりも多くなったときに形成されます。 そして、電子の数が少ないため、イオンによって正電荷が得られます。

陰イオンと陽イオンの両方は、複数の電荷に応じてさらに分割することができます。 そして、上記の用語はすべて単一料金に使用されます。 以下の表では、プラスイオンとマイナスイオンを区別しています。
陽イオンと陰イオンの比較
陽イオン | マイナスイオン | |
定義 | 負に帯電している、すなわちプロトンよりも多くの電子を有する原子または分子。 | 正に帯電している、すなわち電子よりも多くのプロトンを有する原子または分子。 |
ネットチャージ | それは負の実効電荷イオンです。 | それは正の実効電荷イオンです。 |
イオン化 | このプロセスは本質的に発熱性です。 | このプロセスは本質的に吸熱性です。 |
電極 | 電気分解の間に、それは陽極に引き付けられる。 | 電気分解の間に、それは陰極に引き付けられます。 |
によって形成されました | それらは電子を引き付けることによって形成される。 | それらは電子を失うことによって形成されます。 |
とも呼ばれる | 陰イオン | カチオン |
要素タイプ | 非金属 | 金属 |
例 | 硫化物、フッ化物、塩化物、臭化物、ヨウ化物、窒化物および水素化物。 | ナトリウム、鉄、鉛 |