主な違い:分子内の原子の配置は、その極性を決定するのに役立ちます。 分子が正電荷および負電荷を有する場合、その分子は極性であると言われる。 無極性分子は、電荷が少ない分子です。
化学では、極性は、電気双極子または多極子モーメントを有する分子またはその化学基の電荷間の分離を指す。 極性分子は分子間結合と水素結合を介して相互作用します。 分子極性は、分子内の原子間の電気陰性度の差に依存します。 極性は、表面張力、融点と沸点、そして溶解度のような多くの物理的性質も決定します。
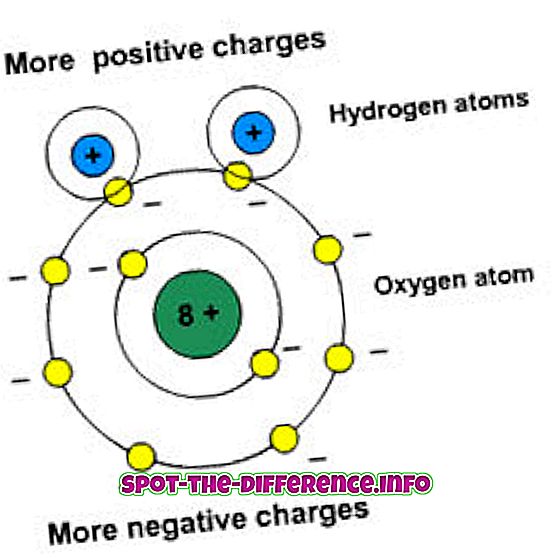
極性は電荷の分離を意味します。 これらの分子は双極子モーメントを持っています。 双極子モーメントは、結合の極性を測定します。 極性物質は他の極性要素と相互作用します。

非極性分子は十分な電荷を持っていません。 非極性分子は対称的に分布しており、それらには多数の電荷を持たない。 2つの原子または2つの同じ原子がそれらの間に同じ電子結合を有する場合、それらの原子は電子対を引き寄せる。 この引っ張りはそれらが電子を共有するのを助け、そして分子間のこの種の結合共有は無極性共有結合として知られている。
極性と非極性の比較
極地 | 非極性 | |
定義 | 極性物質は原子に正電荷と負電荷を持っています。 | 非極性物質は結合原子に大きな電荷を持たない。 |
移動 | それらは電気双極子運動をする。 | 彼らはどんな双極子運動も持っていません。 |
電荷分離 | 電荷分離があります。 | 電荷分離はありません。 |
インタラクション | それらは他の極性物質と相互作用します。 | それらは他の極性物質と相互作用しません。 |
例 | 水、アルコール、硫黄 | 油。 |