主な違い:原子は、すべての問題を構成する基本単位です。 原子は非常に小さく、幅は0.1から0.5ナノメートルです。 あらゆる元素の各原子は、陽子、中性子、および電子で構成されています。 異なる元素の原子が集まって分子を作ります。 これは化学反応によって起こります。 分子とは、存在することができる最小量の化学物質です。
元素は、原子番号で区別される1つまたは1つのタイプの原子を持つ純粋な化学物質です。 原子番号は、元素の核に存在する陽子の数から導き出されます。 同定された合計118の元素があり、それらは金属、半金属および非金属に分けられます。 各要素には独自のプロパティセットがあります。 核反応によって人工的に開発されたものもありますが、ほとんどの元素は地球上で入手可能です。 要素はすでに最も太い形式になっており、さらに細かく分割することはできません。 すべての元素は原子番号でリストされている周期表にあります。
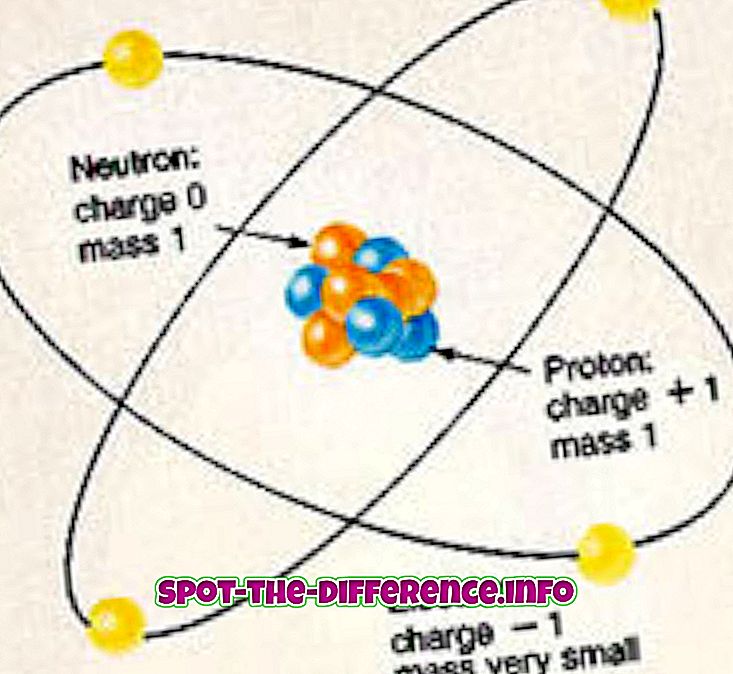
あらゆる元素の各原子は、陽子、中性子、および電子で構成されています。 陽子と中性子は原子の核を構成し、原子の中央に位置しています。 核は電磁力によって核に束縛された電子の雲に囲まれています。 核内の陽子が正電荷を持っているので、電子は負電荷を持っています。 中性子は、その一方で、電荷を持っていません。
原子内の陽子、中性子、電子の数によって、それがどの元素であるかが決まります。 例えば、鉄の原子には26個の陽子、30個の中性子、26個の電子があります。 鉄の各原子はこの配置を持ちます。
異なる元素の原子が集まって分子を作ります。 これは化学反応によって起こります。 例えば、2つの水素原子と1つの酸素原子が結合して水分子を作ります。

分子は、それが作られている要素とは非常に異なる特性を持つことができます。 たとえば、水は、2つの水素原子と1つの酸素原子で構成されていますが、酸素または水素とはまったく異なる動作をします。
さらに、原子は、何かに結合しない限り、自然界で独立して存在することはできません。 単一の酸素原子や単一の炭素原子だけが見つかることはありません。 それは常にO2(酸素)やCO2(二酸化炭素)のようなものと結合しています。 分子に結合すると、その分子は自然に独立して存在することができるため、酸素分子、二酸化炭素分子、水分子(H2O)などを常に見つけることができます。
分子内では、原子は特定の形状または形態で互いにくっついています。 これは主に原子が作ることができる結合の数に依存しています。 原子は互いに化学結合を形成することによって分子を形成します。 酸素原子は常に他の原子と2つの結合を持ち、炭素原子は常に他の原子と4つの結合を持ち、窒素原子は常に他の原子と3つの結合を持ちます。 これにより、特定の種類の分子は常に五角形、六角形、横方向、二方向などの特定の形状を有する。
分子は常に一緒になる傾向があり、それらの形成はそれらの状態に依存します。 気体状態などでは、分子が飛んでいる傾向があります。 液体状態では、分子はまだ動くことができるようにゆるくまとめられている傾向があります。 一方、固体状態では、分子同士は密集しており、振動しかできません。
分子は通常分子式で表されます。 例:O 2、H 2 O、CO 2、C 6 H 12 O 6(砂糖)。 分子式は、要素の名前とそれに続く分子内のその要素の原子数です。